第二节 急性间质性肺炎
急性间质性肺炎(acute interstitial pneumonia,AIP)是指急性起病,发病1个月内出现原因不明的呼吸衰竭,肺内弥漫性肺损伤。1986年Katzen和他的同事报道了8例原因不明的急性呼吸衰竭、肺部出现间质性肺炎的病例,与其他慢性间质性肺炎不同,并且提出了急性间质性肺炎的概念。实际上早在1935年和1944年,Hamman和Rich[1]报道了一组原因不明的病例,其表现为急性起病、初表现为上呼吸道感染样的呼吸道症状,可有发热、咳嗽,继之出现进行的呼吸困难、呼吸衰竭,2~6个月内死亡。病理包括肺水肿、透明膜形成及间质的纤维组织增生。当时命名为急性弥漫性的间质纤维化,之后人们称之为Hamman-Rich综合征。Olson认为Hamman-Rich综合征实质上为急性间质性肺炎。由于其与急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)在病理学上难鉴别,有些文献将其等同于临床上原因不明的急性呼吸窘迫综合征。儿童病例报道远较成人为少[2]。

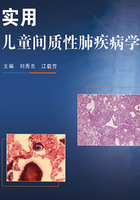
图5-1 急性间质性肺炎病理图(HE染色,×40倍)男,10岁,因咳嗽伴气促乏力10余天入院,入院后患儿呼吸困难,出现Ⅱ型呼吸衰竭。图中可见弥漫性肺泡损伤,肺泡腔内有泡沫细胞渗出
【病理】
急性间质性肺炎组织学上为弥漫性肺泡损伤(图5-1)。大多数的AIP的病理在弥漫性肺损伤的机化期与取活检的时机有关。AIP病理改变为急性期(亦称渗出期)和机化期(亦称增殖期)[3]。急性期为发病后1~2周,其病理特点为肺泡上皮乃至上皮基底膜的损伤,炎性细胞进入肺泡腔内,在受损的肺泡壁上可见Ⅱ型上皮细胞再生并替代Ⅰ型上皮细胞,可见灶状分布的由脱落的上皮细胞和纤维蛋白所构成的透明膜充填在肺泡腔内。另可见肺泡隔的水肿和肺泡腔内出血。此期在肺泡腔内逐渐可见纤维母细胞成分,进而导致肺泡腔内纤维化。机化期多发生在2~3周内,其病理特点是肺泡腔内及肺泡隔内呈现纤维化并有显著的肺泡壁增厚。其特点为纤维化为活动的及主要由增生的纤维母细胞和肌纤维母细胞组成,伴有轻度胶原沉积。此外,还有细支气管鳞状上皮化生。
【临床表现】
AIP发病无明显性别差异,平均发病年龄49岁,年龄从7~77岁均有报告[4]。起病急剧,表现为咳嗽、呼吸困难,即之很快进入呼吸衰竭,类似ARDS。多数病例AIP发病前有“感冒”样表现,半数患者有发热。常规实验室检查无特异性。AIP病死率极高。
【影像学表现】
急性间质性肺炎的CT表现(图5-2)主要为弥漫的磨玻璃影和含气腔的实变影[4-5]。Johkoh等[6]的报道中,36例患者中均有区域性的磨玻璃改变,见牵拉性的支气管扩张。33(92%)例有含气腔的实变,且区域性的磨玻璃改变和牵拉性的支气管扩张与疾病的病程有关。笔者医院的3例患者的肺高分辨CT均为广泛的磨玻璃影和含气腔的实变影,与文献报道的急性间质性肺炎的影像学的特点一致。文献认为牵拉性的支气管扩张在AIP具有特异性,是其他形式的急性肺弥漫性疾病所罕见的[5-6]。并且存活者中合并牵拉性的支气管扩张的比例明显较为未存活者少[7]。

图5-2 急性间质性肺炎CT图
男,10岁,病理诊断为急性间质性肺炎。入院后4天肺CT可见两肺弥漫的磨玻璃改变、实变影(A)、牵拉性支气管扩张(B)
磨玻璃影往往代表病变的可逆性或可治疗性。在急性间质性肺炎时,急性渗出期、亚急性增殖期和慢性纤维化期均可有磨玻璃影的存在,急性渗出期反映肺泡间隔的水肿和透明膜的形成。亚急性的增殖期反映肺泡内和间质的机化。慢性纤维化期代表肺泡间隔的纤维化。因此,急性间质性肺炎时磨玻璃影不能反映病变的可逆性,但急性期的磨玻璃影为可逆的,对激素治疗有效。有文献比较死亡的和存活的AIP的高分辨CT[7],将肺CT分为6个等级:①正常;②磨玻璃影;③实变;④磨玻璃影合并牵拉性支气管扩张或支气管扩张;⑤实变合并牵拉性支气管扩张或支气管扩张;⑥蜂窝肺。发现存活者的肺CT等级分明显较未存活者为低,且存活者的肺磨玻璃影或肺实变合并牵拉性支气管扩张或支气管扩张的范围明显较未存活者为轻。文献研究还发现,肺磨玻璃影或肺实变合并牵拉性支气管扩张组织病理为弥漫性肺泡损伤的纤维化期或机化的晚期,因此预后差。而肺磨玻璃影或肺实变未合并牵拉性支气管扩张为弥漫性肺泡损伤的渗出期或早期纤维化期。
【诊断】
多根据急性起病,发病1个月内出现呼吸衰竭、肺内弥漫性肺损伤,原因不明而诊断。其诊断标准如下[4,8]:无慢性肺病的病史或以前无影像学的肺部异常,无引起ARDS的已知因素如感染、结缔组织疾病、环境或职业的中毒因素、毒物、放射和以前的间质性肺疾病。无近期休克或应用血管加压药史。抗生素、抗病毒治疗无效。
【鉴别诊断】
1.感染性的急性弥漫性肺泡损伤
脓毒血症、各种病原的重症肺炎均可引起急性弥漫性肺泡损伤,但有感染因素;而急性间质性肺炎的原因不明,不能确定感染因素。
2.结缔组织疾病
诊断特发性AIP,一定要排除结缔组织疾病,系统性红斑狼疮、全身类风湿关节炎均可以表现为急性弥漫性肺泡损伤[9]。结缔组织疾病多有肺外的表现,肾和关节的受损。
3.急性过敏性肺炎
急性过敏性肺炎可起病急,出现呼吸困难,临床应该与急性间质性肺炎鉴别。因此,要询问有无引起过敏性肺炎的环境因素。因为过敏性肺炎的病理多以细支气管为中心的间质炎,但一半以上有肉芽肿的存在。急性间质性肺炎的病理为弥漫性肺泡损伤与过敏性肺炎的病理不符。临床急性过敏性肺炎脱离环境因素后,症状会自行改善,也与急性间质性肺炎的临床表现不同。
4.特发性肺纤维化的急性加重
特发性肺纤维化可急性加重,突然出现呼吸衰竭,但多数根据肺病的病史可初步鉴别。AIP的病理均为弥漫性的肺泡损伤,并无蜂窝肺的表现,因此可与特发性肺纤维化的急性加重鉴别。
5.非特异性的间质性肺炎
弥漫性肺泡损伤的吸收期,在病理上有时也不易与NSIP的病理鉴别。因此,医生可根据其发病急缓,有无呼吸衰竭来进一步鉴别。
6.急性嗜酸性粒细胞性肺炎
起病急,呼吸困难,病情相对较重,可引起呼吸衰竭,影像学主要为区域性的磨玻璃影[10],部分有含气腔的实变影。因此,应该与急性间质性肺炎鉴别。支气管肺泡灌洗液中嗜酸性粒细胞的增加可做出诊断[11]。用激素治疗见效快。肺活检可见大量的嗜酸性粒细胞是其特点。
7.BOOP
BOOP在影像学上与AIP有一致之处为高分辨CT均为含气腔的实变影,BOOP多在外周性分布,且无牵拉性支气管扩张。病理上,BOOP以细支气管周围炎症、腔内的纤维化为著,而AIP的病理表现为弥漫性肺泡损伤,且每一视野均一致,与BOOP的病理肺泡腔内机化、片状分布而不同。临床起病急,出现呼吸衰竭可进一步排除BOOP。对急进性的BOOP可通过支气管肺泡灌洗液中无淋巴细胞增高而鉴别[5]。
【治疗】
AIP治疗上无特殊方法,可采用ARDS治疗方法。AIP死亡率极高[12-14],如果除外尸检诊断的AIP病例,死亡率可达50%~88%(平均62%),平均生存期限短,多在1~2个月死亡。激素可加速弥漫性肺泡损伤的机化期修复,因此在早期机化期有效。这表明激素治疗的有效性与治疗的早晚有关。多数文献报道,大剂量的激素冲击治疗效好[15]。也有报道早期的机械通气可改善急性间质性肺炎的预后[8]。成人急性间质性肺炎也有较低死亡率的报道[16]。北京儿童医院有3例诊断为急性间质性肺炎应用激素得到成功的治疗[3]。
(刘秀云 江载芳)
参考文献
1.Hamman L,Rich AR.Acute diffuse interstitial fibrosis of the lungs.Bull Johns Hopkins Hosp,1944,74:177.
2.Kwong SY,Kim JM,Sohn MH,et al.acute interstitial pneumonia in siblings:A case report.JKorean Med Sci,2008,23(3):529-532.
3.刘秀云,江载芳,周春菊,等.小儿急性间质性肺炎三例及文献回顾.中华儿科杂志,2011,49(2):98-102.
4.American Thoracic Society,European Respiratory societ.American Thoracic Society/European Respiratory society Internationalmultidisciplinary consensus classification of the idiopathic interstitial pneumonias.Am J Respir Crit Care Med,2002,165:277-304.
5.Bonaccorsi A,Cancellieri A,Chilosi MR,et al.Acute interstitial pneumonia:report of a series.Eur Respir J,2003,21(1):187-191.
6.Johkoh T,Muller NL,Taniguchi H,et al.Acute interstitial pneumonia:Thin-section CT findings in 36 patients.Radiology,1999,211(3):859-863.
7.Ichikado K,suga M,Muller SN etal.Acute interstitial pneumonia:comparison of high resolution computed tomography findings between survivors and nonsurvicors.Am J Respire Crit Care Med,2002,165:1551-1556.
8.Suh GH,Kang EH,Chung MP,etal.Early intervention can improve clinical outcome of acute interstitial pneumonia.Chest,2006,129(3):753-761.
9.Parambil JG,Myers JL,Aubry MC,et al.Causes and prognosis of diffuse alveolar damage diadnosised on surgical lung biopsy.Chest,2007,132(1):50-57.
10.Daimon T,Johkoh T,Sumikawa H,et al.Acute eosinophilic pneumonia:Thin-section CT findings in 29 patients.Eur J Radiol,2008,65(3):462-467.
11.Philit F,Etiennemastroïanni B,Parrot A,et al.Idiopathic acute eosinophilic pneumonia.Am J Respir Crit care Med,2014,26(9):373-376.
12.Vourlekis JS,Brown KK,Cool CD,et al.Acute interstitial pneumonitis:case series and review of the literature.Medicine(Baltimore),2000,79(6):369-378.
13.Avnon LS,Pikovsky O,Sion-Vardy N,et al.Acute interstitial pneumonia-Hamman-Rich syndrome:clinical characteristics and diagnostic and therapeutic considerations.Anesth Analg,2009,108(1):232-237.
14.Bouros D,Nicholson AC,Polychronopoulos V,et al.Acute interstitial pneumonia.Eur Respire J,2000,15(2):412-418.
15.王京岚,陈毅德,孙庆华,等.急性间质性肺炎附一例报告.中华内科杂志,1997,36(11):744-747.
16.Quefatieh A,Stone CH,Digioxine B,et al.Low hospital Mortality in patients with acute interstitial pneumonia.Chest,2003,124(2):554-559.